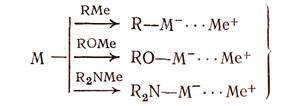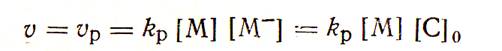|
Контрольная работа: Высокомолекулярные соединенияКонтрольная работа: Высокомолекулярные соединения1. Опишите основные закономерности процесса анионной полимеризации: механизм, катализаторыПолимеризация по ионному механизму происходит на анионных активных центрах, когда концевой атом растущей полимеризационной цепи обладает отрицательным зарядом, т.е. представляет собой карбанион (с положительным противоионом). Анионные системы очень чувствительны даже к небольшим количествам примесей веществ, способных разрушить активные анионные центры (вода, спирты и др.). Поэтому использование анионной полимеризации в промышленности затруднено. Несмотря на это по ионному механизму ведут процессы получения синтетических каучуков, полимеризации капролактама, формальдегида. Возникающие трудности перекрываются высокой производительностью анионных процессов и возможностью получать полимеры с некоторыми специфическими свойствами. Вследствие большой концентрации активных центров скорость анионной полимеризации в 104 – 107 раз выше скорости радикальной полимеризации. /5, c. 426/ Анионными инициаторами являются доноры электронов. Инициирование можно осуществлять двумя путями: 1. Прямой атакой инициатора на молекулу мономера с образованием карбаниона (нуклеофильное инициирование); 2. Передачей (переносом) электрона от молекулы донора на двойную связь мономера с образованием анион-радикала. Нуклеофильное инициирование осуществляется при взаимодействии полярного соединения основного характера с непредельной связью мономера с образованием активного центра в виде ионной пары (реже, свободного карбаниона):
В качестве инициаторов этого типа можно использовать металлалкилы, алкоксиды (алкоголяты) и амиды металлов (Me):
Реакционная способность анионного инициатора связана с ионностъю его активной связи (например, R—Ме). Однако относительная активность в реакции инициирования зависит не только от ионности связи RMe, но и от реакционной способности карбаниона. Так, в алкоксидах металлов ROMe связь кислород — металл более ионная, чем связь углерод — металл в металлалкилах RMe, но реакционная способность ROMe по отношению к ненасыщенным мономерам значительно ниже (например, они совсем не полимеризуют диеновые углеводороды), чем у RMe. В некоторых случаях, например у широко применяемых литийорганических соединений, в неполярных средах соединения RLi (R — неполярный заместитель) представляют собой ассоциаты типа (RLi)n с коэффициентом п = 2—6, образующие равновесную си-хтему из различных .диссоциированных форм. /5, c. 423/. Алкоксиды ROMe также образуют подобные ассоциаты (с я = = 9), которые устойчивы и в полярных растворителях при повышенной температуре. Естественно, что ассоциированные формы менее реакционноспособны, чем мономерные. Если анионную полимеризацию ненасыщенных углеводородов проводить в условиях, исключающих обрыв цепи, то ее рост может продолжаться практически до полного израсходования всего мономера, причем на конце полимерных цепей будет сохраняться активный анионный центр, способный к дальнейшей реакции полимеризации (например, при добавлении в реакционную смесь новых порций мономера). Такие устойчивые макроанионы поэтому называют живущими полимерами. Они образуются в растворителях, не способных к реакциям передачи цепи (тетрагидрофуран, диоксан, 1,2-диметоксиэтан). Кинетика образования живущих полимеров зависит в простейшем случае от соотношения констант скоростей реакций инициирования и роста (kp) цепи. При условии kи >>kp скорость реакции в системах без обрыва цепи будет соответствовать скорости роста:
где [M-] — общая концентрация живущих анионных центров, которая гари полном отсутствии в системе агентов передачи цепи соответствует исходной концентрации инициатора (катализатора) [С]о. При kи >>kp возможно образование живущих полимеров с очень узким молекулярно-массовым распределением (например, распределение Пуассона), т. е. с очень однородным полимергомологическим составом. В случае kи <<kp процесс идет нестационарно и уравнение справедливо только после завершения реакции инициирования, а образующиеся полимеры имеют широкое молекулярно-массовое распределение. 2. Модификация ВМС. Деструктивные процессы полимеров, их использование для получения сополимеровОдним из наиболее эффективных путей модификации свойств высокомолекулярных соединений является сополимеризация. Для получения полимеров с модифицированными свойствами различных гополимеров, используют несколько (обычно два или три) разных мономеров, проводя реакцию их сополимеразации. Изменяя состав сополимера, можно влиять на растворимость. /4, c. 78/ Сополимеры, полимеры, макромолекулы которых содержат мономерные звенья нескольких типов. В регулярных сополимерах различающиеся звенья распределяются в определённой периодичности. Простейшие примеры — сополимеры стирола с малеиновым ангидридом и некоторых олефинов с SO2, построенные по принципу... АВАВАВ... (А и В — мономерные звенья различных типов). Более сложные регулярные последовательности чередования звеньев характерны, например, для различных аминокислотных остатков в некоторых белках, например глицин-пролин-оксипролин в коллагене. В нерегулярных сополимеров распределение звеньев случайное, что характерно для многих синтетических сополимеров. В нуклеиновых кислотах и большинстве белков нерегулярные последовательности звеньев задаются соответствующим кодом и определяют биохимическую и биологическую специфичность соответствующих соединений. Сополимеры, в которых звенья каждого типа образуют достаточно длинные непрерывные последовательности (блоки), сменяющие друг друга в пределах макромолекулы, называются блоксополимерами. К внутренним (неконцевым) звеньям макромолекулярной цепи одного химического состава могут быть присоединены одна или несколько цепей др. состава. Такие сополимеры называются привитыми. /1/ Сочетая в одной макромолекуле химические звенья самых различных типов, можно создавать материалы с заранее заданным комплексом свойств. Т. о., синтез сополимеров — один из наиболее эффективных путей модификации свойств высокомолекулярных соединений. Деструкция полимеров - разрушение макромолекул под действием тепла, кислорода, влаги, света, проникающей радиации, механических напряжений, биологических факторов (например, при воздействии микроорганизмов) и др. В соответствии с фактором воздействия различают следующие виды деструкции полимеров.: термическую, термоокислительную, фотохимическую, гидролитическую, радиационную и др. Обычно в полимере одновременно протекает несколько видов деструкционных процессов, например при переработке полимера в изделие - термическая, термоокислительная и механическая. В результате деструкции уменьшается молярная масса полимера, изменяются его строение, физические и химические свойства, т. е. происходит его старение, и он часто становится непригодным для практического использования. Однако не всегда деструктивные процессы — отрицательное явление. Так, этот процесс используют при механосинтезе различных блок- и привитых сополимеров, при пластикации каучуков, для получения из природных полимеров ценных низкомолекулярных веществ (например, глюкозы) и т.д. Изучение деструкции позволяет разработать научные основы и практические методы стабилизации полимеров. Разрыв макромолекулы в поле механических сил механодеструкция — сопровождается возникновением свободных радикалов, способных активизировать и инициировать в определённых условиях химические процессы. Возникновение макрорадикалов наблюдается, например, при дроблении, вальцевании, действии ультразвука и пр. Уменьшение энергии химических связей в полимерных цепях в результате увеличения межатомных расстояний под действием механических напряжений может также активировать процессы окисления, термической, химической и др. видов деструкции полимеров. Механодеструкция сопровождается значительным изменением всего комплекса физико-химических свойств полимера — уменьшением молекулярной массы, появлением новых функциональных групп, изменением растворимости, возникновением системы пространственных связей и т.д. Наряду с этим механическое воздействие на системы из нескольких полимеров или полимера и мономеров позволяет осуществить синтез новых полимеров, блоки привитых сополимеров (механо-синтез) в результате взаимодействия макрорадикалов различного строения друг с другом или с мономерами. Механохимические превращения используются для направленного изменения свойств полимеров (пластикация каучуков), получения новых полимерных материалов (ударопрочные полистирол и поливинилхлорид), для восстановления пространственных структур (регенерация вулканизатов). В то же время механохимические явления во многом способствуют развитию процессов утомления и разрушения полимерных тел, а эти процессы определяют возможность эксплуатации изделий из полимерных материалов. Поэтому большое значение имеет стабилизация полимеров, особенно при длительных циклических нагрузках (с этой целью, например, в рецептуры резиновых смесей вводят противоутомители). 3. Характеристика агрегатных и фазовых состояний ВМСПолимеры в твердом состоянии могут быть аморфными и кристаллическими. При нагревании аморфного полимера наблюдают три физических состояния: стеклообразное, высокоэластичное и вязкотекучее. Эти состояния устанавливают на основании кривой термомеханического состояния. Аморфный полимер находится ниже температуры стеклования (Тс) в твердом агрегатном состоянии. При температуре выше Тс полимер находится в высокоэластичном состоянии; молекулярная подвижность при этом становится настолько большой, что структура в ближнем порядке успевает перестраиваться вслед за изменением температуры, а макромолекулы могут изгибаться под действием внешних сил. Общая деформация складывается в этом случае из упругой и запаздывающей высокоэластичной деформации. При упругой деформации изменяются средние межцентровые, межмолекулярные расстояния и валентные углы в полимерной цепи, при высокоэластичной деформации изменяется ориентация и перемещаются на значительные расстояния звенья гибких цепей. Кристаллизующийся полимер в зависимости от скорости охлаждения расплава полимера может проявлять два вида структур: аморфную и кристаллическую. При медленном охлаждении кристаллизующихся полимеров совместная укладка отрезков макромолекул образует структуру макромолекул. Это затрудняет переход их из одной конформации в другую, из-за чего отсутствует гибкость макромолекул и нет высокоэластичного состояния. При быстром охлаждении кристаллические структуры не успевают полностью сформировываться, поэтому в переохлажденном полимере между ними имеется "замороженная" – аморфная структура. Эта аморфная структура при повторном нагреве до температуры выше температуры плавления (Тпл) создает вязкотекучее состояние. Для структуры полимера характерны два состояния: кристаллическое (до температуры плавления) и вязкотекучее (выше температуры плавления). Вязкотекучее состояние, характерное для аморфного и кристаллического состояния полимера, в основном, обеспечивает при течении полимера необходимые деформации путем последовательного движения сегментов. Вязкость полимера увеличивается с увеличением молекулярной массы полимера, увеличивается также при этом и давление формования изделий. /2, c. 135/ Таким образом, высокомолекулярные вещества могут находиться в трех состояниях: стеклообразном, высокоэластичном и вязкотекучем, соответственно разделенных температурами Тс и Тт. Эти состояния могут изменятся в зависимости от температуры, состава среды, условий межцепного взаимодействия. 4. Концентрированные растворы ВМС. Основные свойства и применение Растворы ВМС - являются истинными растворами, а это значит, что они представляют собой гомогенные системы, в которых взвешенные частицы не содержат ядер. Здесь, взвешенные частицы представлены макромолекулами – молекулами гигантских размеров. Таким образом, макромолекулы являются ответственными за большинство физических свойств растворов ВМС, которые сильно отличаются от свойств низкомолекулярных соединений. Строение микромолекул, в свою очередь, также оказывает сильное влияние на поведение растворов ВМС. Одной из главных особенностей ВМС является, так называемый процесс денатурации - специфическое необратимое осаждение белков. Он происходит при действии высоконцентрированных кислот и щелочей, дубильных веществ, под влиянием высокой и низкой температур, механического воздействия высокого давления, ультразвука, лучистой энергии. К основным высокомолекулярным соединениям относятся белки, целлюлоза, нитроцеллюлоза, каучук, желатин и др. Растворы ВМС - всегда термодинамически устойчивые системы, способные существовать без стабилизатора неограниченное время в весьма больших массовых и значительных молярных концентрациях. Они образуются самопроизвольно, с уменьшением свободной энергии. Если в качестве диспрессионной среды использовать такую жидкость, по отношению к которой данное высокомолекулярное вещество явл. лиофобным (не способным в нем раствориться), ВМС способны образовывать не только растворы, но и типичные лиофобные золи. В то же время растворы ВМС представляют собой равновесные системы, к которым применимо правило фаз, в отличие от лиофобных коллоидов. Растворы ВМС, так же, как растворы низкомолекулярных соединений, могут быть как молекулярными, так и ионными. В ионных растворах ВМС природа зарядов связана с наличием функциональных групп. Повышенная вязкость растворов ВМС связана с формой макромолекул и характером межмолекулярных взаимодействий и объясняется большой сольватацией макромолекул. Вязкость растворов высокомолекулярных соединений, обычно выше вязкости растворов низкомолекулярных соединений и коллойдных растворов, взятых с одинаковой концентрацией. При исследовании растворов ВМС характеристическую вязкость обозначают через [h]. Причиной отклонения вязкости растворов ВМС является взаимодействие вытянутых и гибких макромолекул, часто образующих структированные системы. Такие системы получили название ассоциаты. Ассоциаты обладают свойством сильно увеличивать вязкость растворов. Явление светорассеяния и спектры поглощения ВМС В исследовании твердых полимеров важную роль играют инфокрасные спекторы поглощения ВМС. К сожалению они очень сложны для использования при исследовании самих растворов ВМС. Кроме того растворы ВМС характеризуются светорассеянием. Это свойство, изменение величины рассеяния света, чрезвычайно полезно для различных научных исследований. В частности, используется в методе определения относительной массы полимеров, т.к. цепные молекулы полимеров нельзя обнаружить в растворах при ультрамикроскопических наблюдениях. Метод основан на измерении мутности разбавленных растворов ВМС. Появление на поверхности молекул заряда, является одной из важных проблем, возникающих при изучении ВМС. Возникновение заряда объясняется рядом причин. Например, поверхность ВМС может иметь собственный заряд, возникающий благодаря расположенным на ней анионным и катионным группам. Наличие заряда у крупных частиц, может служить отличием ВМС от низкомолекулярных соединений. При электрофорезе заряженная частица, присутствующая в растворе, в частности микромолекула, под действием электрических сил движется к электроду противоположного знака. Это свойство часто используют, когда необходимы доказательства наличия заряда у частицы ВМС. Для белков между зарядом молекул и электрофоретической подвижностью существует прямая пропорциональная зависимость в широком интервале рН. Изоэлектрической точкой – называют значение рН, при котором лектрофоретическая подвижность белка равна нулю. При значении рН, близком к изоэлектрической точки, разноименно заряженное группы -NH3+ и COO- притягиваются друг к другу и нить закручивается в спираль. Тогда раствор имеет наименьшую вязкость. Молекулы ВМС в развернутом состоянии придают растворам более высокую вязкость. Если молекула белка ведет себя как основание, приобретает положительный заряд и при электрофорезе движется к катоду, то эта среда кислая ( когда в результате избытка водородных ионов подавлена ионизация карбоксильных групп). Если же молекула белка ведет себя как кислота и при электрофорезе передвигается к аноду - среда щелочная (подавлена ионизация аминогрупп). В изоэлектрическом состоянии свойства растворов белков резко меняется: при этом они имеют, наименьшую вязкость, плохую растворимость. Процесс поглощения ВМС больших объемов низкомолекулярной жидкости, сопровождающейся значительным увеличением объема ВМС, называется набуханием. На первой стадии взаимодействия ВМС и низкомолекулярной жидкости, образуется Гетерогенная система, состоящая из ВМС и свободной низкомолекулярной жидкости. Процесс проникновения молекул растворителя в макромолекулы ВМС приводит к тому, что при набухании объем полимера всегда увеличивается, а объем всей системы уменьшается. Уменьшение объема системы при набухании, называемая контракцией. При набухании происходит диффузия молекул растворителя в высокомолекулярное вещество. Это обусловлено двумя факторами: 1. Достаточно большими промежутками между макромолекулами ВМС. 2. Большей подвижностью маленьких, по сравнению с макромолекулами ВМС, молекул растворителя. В результате поглощения растворителя макромолекулами ВМС, увеличивается плотность системы. Процесс растворения ВМС можно разделить на четыре стадии: 1. Начальная стадия. Система гетерогенна и двухфазна. Представляет собой чистую низкомолекулярную жидкость и чистый полимер Ж1 + Ж2. 2. Стадия набухания. На этой стадии система расслаивается на две жидкие фазы. Одна фаза – раствор низкомолекулярного компонента в компоненте ВМС. Вторая фаза - чистая низкомолекулярная жидкость. Ж1 → Ж2, где Ж2 – набухший ВМС, а Ж1 чистая низкомолекулярная жидкость. 3. Стадия образования второго раствора Ж2 → Ж1 . Жидкий растворитель дифуззирует в полимер. 4. Стадия полного растворения – превращение гетерогенной (двухфазной) системы в галогенную Ж1 → Ж2. Процесс набухания характеризуется увеличением объема набухшего тела. Если создать препятствие увеличению объема набухающего тела, то при этом развивается давление, давлением набухания pH .
где K – константа, зависящая от природы полимера и растворителя; n – константа, почти не зависящая от стиля природы последних и в среднем приблизительно равна 3; С – концентрация выраженная в кг сухого ВМС в 1м3 образовавшаяся системы. Существуют ограниченное и неограниченное виды набухания. Ограниченное – набухание не переходит со временем в полное растворение, а останавливается на второй или третьей стадии. Примером может служить набухание при комнатной температуре желатина. Неограниченное набухание представляет непрерывный процесс, переходящий через все четыре стадии и заканчивающийся полным растворением. Образуется однофазная система. Например, так набухают каучуки в бензоле, нитроцеллюлоза в ацетоне, белок в воде, целлюлоза в ацетоне. Изменение растворимости ВМС может быть вызвана либо понижением температуры, либо изменением состава раствора путем добавления жидкости, в которой ВМС не растворяется. Все процессы нарушения устойчивости растворов ВМС связаны с переходом от полного растворения ВМС к ограниченному растворению или к нерастворимости. Введением в раствор электролитов, напрямую связано с нарушение устойчивости растворов ВМС. Механизм коагуляции лиофобных коллоидов и нарушение устойчивости ВМС различны по своему действию, т.к. коагуляция золей происходит при введении малых концентраций электролита и представляет собой обычное необратимое явление. При добавлении в раствор ВМС электролита наблюдается эффект высаливания, что объясняется уменьшением растворимости ВМС в концентрированном растворе электролита. 5. Ориентационная вытяжка волоконУпрочнение полимеров обычно достигается путем создания в них такой структуры, которая обеспечивает более равномерное распределение внешней нагрузки по макромолекулам. Для гибкоцепных полимерных волокон основным способом упрочнения является ориентационная вытяжка, заключающаяся в растяжении волокон внешней силой при повышенной температуре (выше температуры стеклования) /1/. Возникающая при этом параллельная укладка цепей фиксируется при понижении температуры за счет стеклования и кристаллизации. При анализе процесса ориентационной вытяжки можно прийти к следующему заключению: внутренний порядок создает не сама растягивающая сила, но она задает энергетически выгодное преимущественное направление в системе. Выстраивание же цепей вдоль этого направления обеспечивает тепловое крупномасштабное сегментальное движение гибких макромолекул. Цепи в полимере перепутаны, и при „распутывании узлов" участкам макромолекул приходится перемещаться и в направлениях, не совпадающих с направлением внешней силы /2, c. 48/. Для эффективного упрочнения гибкоцепных полимеров важно оптимальное соотношение между скоростями растяжения и интенсивного сегментального движения. При этом существенную роль играет обнаруженный С.Н. Журковым /3, c. 78/ эффект „механического стеклования" — торможение сегментального движения в поле внешней растягивающей силы. Учет этого эффекта позволяет установить количественную связь между кратностью вытяжки и скоростью растяжения гибкоцепных кристаллизующихся полимерных волокон /4, c. 65/. Сегментальное движение макромолекул широко исследуется теоретически и экспериментально /3, c. 115/.Список литературыШестакова КС, Касьянова А.А Химия и физика высокомолекулярных соединений в производстве искусственной кожи, кожи и меха - М: Легкая индустрия, 1976,-528 с Касьянова А А. Добрынина Л.Е Лабораторный практикум по физике и химии высокомолекулярных соединений, - М.: Лакая индустрия.. 1979. -176 с, Роговин ЗА Основы химии и технологии химических волокон.- М: Химия, 1974.-т.1и2, Бобович Б.Е Свойства, модификация и применение термоэластопластов, -М: МИГЭИжгпром, 1975-57с Сорокин М.Ф. Химия и технология пленкообразующих веществ. – М.: химия, 1981. |
|
|
| 17.06.2012 |
| Большое обновление Большой Научной Библиотеки |
| 12.06.2012 |
| Конкурс в самом разгаре не пропустите Новости |
| 08.06.2012 |
| Мы проводим опрос, а также небольшой конкурс |
| 05.06.2012 |
| Сена дизайна и структуры сайта научной библиотеки |
| 04.06.2012 |
| Переезд на новый хостинг |
| 30.05.2012 |
| Работа над улучшением структуры сайта научной библиотеки |
| 27.05.2012 |
| Работа над новым дизайном сайта библиотеки |